Estados de la Materia
En el número anterior estudiamos sobre la materia, ahora vamos a ver sobre los estados en los que la podemos encontrar en la naturaleza, estos son:
- - Sólido.
- - Líquido.
- - Gaseoso.
Estos estados dependen del comportamiento de las moléculas en cada uno de los cuerpos.
Las moléculas son las partículas más pequeñas de un cuerpo que conserva las mismas características: estas son su naturaleza, propiedades físicas y químicas. Por lo tanto, una molécula de azufre tendrá el mismo olor, color, sabor, etc., que un gran trozo de azufre.
Recordemos que las moléculas están formadas por átomos que están unidos eléctricamente entre sí, es decir por medio de sus electrones. Por ejemplo: Una molécula de agua está formada por dos átomos de hidrógeno y uno de oxígeno.
Todos hemos estado en contacto con el agua y la encontramos en su mayor parte en forma líquida, como el agua que bebes de un vaso; pero qué pasa si el agua de ese vaso lo pones a hervir en una olla, sale un vapor y ese es otro estado del agua, el gaseoso. Ahora, si esa agua del vaso lo pones en un recipiente plástico en el congelador, se hace hielo y ese es el otro estado del agua, sólido. Advertencia: no pongas líquidos a congelar en vasos de vidrio porque se parten.
Bueno, como puedes notar, hay tres estados de la materia: sólido, líquido y gaseoso. Pero lo más importante es que los pudiste cambiar variando la temperatura, de líquido a gaseoso aplicando calor y de líquido a sólido aplicando frío. Esto tiene una explicación: El calor dilata los cuerpos y el frío los contrae, por está razón el calor separó las moléculas de agua y cambió su estado de líquido a gaseoso, mientras que el frío unió las moléculas de agua y modificó su estado de líquido a sólido.
Podemos concluir, que los estados de la materia pueden cambiar al variar su temperatura, con altas temperaturas (aplicando calor) los podremos pasar de sólido a líquido y luego a gaseoso y con bajas temperaturas (enfriándolos) de gaseoso a líquido y luego a sólido. También que en los sólidos las moléculas están muy unidas, en los líquidos más separadas y en los gases mucho más. La fuerza que mantienen unidas a las moléculas se conoce como COHESIÓN y no es igual en todos los cuerpos y estados en que se encuentran.
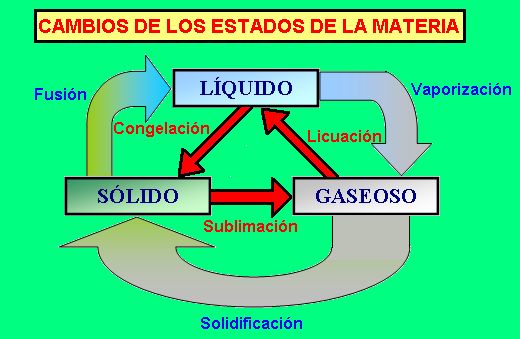
CAMBIOS DE LOS ESTADOS DE LA MATERIA
Como hemos dicho la materia se presenta en tres estados: sólido, líquido y gaseoso. Pero ésta puede cambiar de un estado a otro, a estos procesos se los define de la siguiente manera:
- - Congelación: Es el cambio del estado líquido al sólido.
- - Sublimación: Es el cambio del estado sólido al estado gaseoso.
- - Licuación: Es el cambio del estado gaseoso al estado líquido.
- - Vaporización: Es el cambio del estado líquido al estado gaseoso.
- - Solidificación: Es el cambio del estado gaseoso al estado sólido.
- - Fusión: Es el cambio del estado sólido al estado líquido.
Ahora estudiemos las características de los cuerpos, en estado sólido:
- - Su consistencia es más o menos dura.
- - Aunque no lo notemos sus moléculas se mueven muy lentamente, no lo hacen rápidamente debido a que la cohesión entre sus moléculas es tan fuerte que dificulta su movimiento y las mantiene unidas.

En el líquido:
- - Su consistencia es blanda y toma la forma del recipiente que lo contiene.
- - Las moléculas se mueven con mayor rapidez y esto es lo que precisamente no permite que un líquido tenga forma determinada.
- - A los líquidos también se los llama fluidos, porque la poca cohesión entre sus moléculas y el no poder apartarse unas de otras, le dan esta característica especial de fluidez.

En los gases:
- - No existe cohesión, por lo que sus moléculas tienden a separarse unas de otras.
- - Al no haber una fuerza que una sus moléculas, éstas se separan y ocupan un lugar ilimitado, por lo que carecen de forma.

Como lo dijimos en un párrafo anterior, al aplicar calor las moléculas de un cuerpo se separan, en el caso del agua se puede pasar del estado sólido, al líquido y luego al gaseoso, en este último estado sus moléculas al perder atracción mutua se escapan y se pierden en la atmósfera. Esto es lo que pasa en cuando el sol calienta el hielo de los glaciares, los derrite y los convierte en agua. También cuando la ausencia del sol hace que se enfríe el agua y se congele.
En tu casa debes haber experimentado el fenómeno de licuación, puesto que en el aire hay moléculas de agua libres y al poner una botella de jugo helado tapado o cerveza helada, debes haber notado como se humedece el exterior de la botella. Lo que ocurre es que el frío de la botella helada hace que las moléculas de agua se agrupen en forma de gotitas (pasando el agua de estado gaseoso a líquido). También al hervir el agua, no solamente has observado el cambio del agua del estado líquido a gaseoso, sino que si pones la tapa de la olla encima de ese vapor, notas como aparecen gotitas en la tapa, esto se debe a que la tapa enfría el vapor de agua y lo cambia de estado gaseoso a líquido. Esto también se observa cuando se cocina arroz y al destapar la olla, aparece mojada su tapa.

Cuando la materia está en estado gaseoso carece de volumen, cuando pasa a líquido el volumen lo adopta del recipiente que lo contiene y en estado sólido tiene un volumen definido. Al cambiar los estados de gaseoso a líquido o de líquido a sólido, la materia se hace más densa (más compacta). Cuando preparan flan o gelatina en tu casa, debes haber observado como el líquido se transforma en algo sólido por efecto de la temperatura. La temperatura es importante para condensar la materia, condensar es hacer la materia más densa o compacta. La condensación de un gas se obtiene por compresión o enfriamiento y es lo que sucede cuando con la tapa de una olla se enfría el vapor de agua y aparecen las gotitas en la tapa.
En una posterior entrega veremos sobre el ciclo del agua no solamente desde el punto de vista físico, sino también molecular.
Fuente:
Revista Varitek Universal, Año 2 – Número 6, 15 de junio del 2009.
